"comprehendere scire est"
Consejo Nacional para el Entendimiento Público de la Ciencia.
Consejo Nacional para el Entendimiento Público de la Ciencia.
Elsa Verónica Herrera Mayorga + Centro De Biotecnología Genómica, Instituto Politécnico Nacional, Reynosa, Tamaulipas, México
¿Quién es Spodoptera frugiperda?
S. frugiperda (J. E. Smith) es una especie artrópoda perteneciente a la clase insecta del orden Lepidóptera de la familia de los Noctuidos es una plaga polífaga nativa del hemisferio occidental con amplia distri-bución geográfica, desde Argentina y Chile, hasta el sur de Estados Unidos (Alonso Alvarez, 1991, Pastrana y Hernández, 1979, Murillo, 1991), muy fácil de identificar por su daño y puede calificarse como una plaga que causa mayores pérdidas si no se controla en el momento oportuno (Sag y col., 1998), S. frugiperda de acuerdo a la conducta en campo y la importancia se encuentra en el grupo de las plagas constantes, estas son las que están presentes casi siempre y se espera que causen pérdida económica o daño cada año ya que se presentan durante todo el ciclo vegetativo del cultivo, por esto demanda de 3 a 4 aplica-ciones químicas para su control, incre-mentando así los costos de producción y generando efectos indeseables cada año para el ambiente y el ser humano (King y Saunders., 1984, Castro y Suarez., 1999).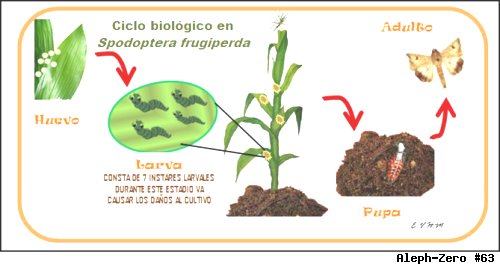
Entre los nombres más comunes tene-mos; gusano cogollero derivado de su forma de daño más conocida que es en el cogollo de la planta o gusano ejército u "oruga militar tardía" ya que si el alimen-to se hace escaso, las larvas se trasladan a otros cultivos desplazándose en masa como un "regimiento" causando de esta manera distintos daños los cuales se van a presentar de forma más severa durante la fase vegetativa inicial del desarrollo de la planta, 30 días después de la siembra, puede llegar a ocasionar perdidas en el rendimiento de un 30 a un 64 %, el ataque se presenta con mayor frecuencia en cultivos como maíz, sorgo, arroz, algodón, soya, girasol y varias especies de pastos, el insecto presenta preferencia en su alimentación por hojas y brotes tier-nos, especialmente de los cogollos con-virtiéndose en un masticador del tejido vegetal, el cual en México ha venido causando pérdidas en la producción y daños más graves en siembras tardías (Willink et al., 1993). Las numerosas pérdidas causadas por S. frugiperda en los cultivos se deben a su poder de aclimata-ción a diferentes condiciones lo cual ha permitido que su distribución geográfica sea amplia (Andrews., 1988; Willink et al., 1993; Artigas., 1994; Virla et al., 1999; Clavijo y Pérez Greiner, 2000; Pogue, 2002).
¿Cómo se reproduce?
Una hembra ovipone un promedio de 1,044 ± 391.8 las cantidades van de 600 a 1500 huevos a lo largo de su vida, los cuales se depositan en masas o grupos compactos que promedian de 100 a 150 huevos cada una (Estrada, 2002; Murúa y Virla, 2004; Murúa et al., 2008). Los lugares en donde estos huevos son depo-sitados no siempre corresponden a la planta que va a servir de alimento para las larvas, ya que cuando ocurren grandes explosiones poblacionales, pueden ser hallados en lugares tan diversos como postes de luz, paredes, alambrados, etc. (Cruz, 1995). Cuando se les encuentra en los cultivos como el maíz, indepen-dientemente de su estado fenológico, son colocados sobre las hojas, en la parte media de la planta, preferentemente en el envés y/o en la zona basal de las mis-mas (Valverde et al., 1995; García Roa et al., 1999; Clavijo y Pérez Greiner, 2000; Murúa et al., 2009). Luego de nacidas, las larvas permanecen agrupadas en la parte baja de las plantas, refugiadas entre las hojas, cada agrupación va durar aproximadamente 3 días. El primer alimento de las mismas es el corion de los huevos, después de lo cual, si el hospede-ro no es el adecuado, migran a través de un hilo de seda en busca de alimento. Las más jóvenes comen durante el día mien-tras que en los últimos estadios son más activas de noche (Casmuz A. et al., 2010; Estrada, 2002).
El período larval dura un promedio de 25 días, pasando generalmente por seis o siete instares larvales (Artigas, 1994; Murúa et al., 2003; Murúa y Virla, 2004a; Murúa et al., 2008). Las larvas de insectos sufren las mudas durante su desarrollo en consecuencia de distintos cambios hormonales, lo cual causa varia-ciones en el tamaño, en su comporta-miento y morfología (Strand., 1990, Gu et al. ,2000), para completar su desarro-llo, las larvas consumen un promedio total de 179.7 cm2 de superficie foliar de hojas de maíz y dejan de alimentarse justo antes de alcanzar el último estadio larval (Rezende et al., 1994). Éstas pasan inad-vertidas hasta que alcanzan 20 a 25 mm, cuando son detectadas por sus daños, expresados en hojas que ya están perfora-das al momento de desplegarse. En sus primeros instares es verde con manchas y líneas negras dorsales, después se vuelve verde o canela brillante, longitudinal-mente con tres líneas dorsales blanco amarillentas, el dorso del octavo segmen-to abdominal, presenta cuatro puntos (pinaculas) negros formando un cuadrado adfrontal claro, sus suturas no alcanzan el triángulo vertical, las mandíbulas con el primer y segundo diente más grande que el otro, va presentar una sutura epicra-neana en forma de “Y” invertida de color amarillo (King and Saunders, 1984; Estrada, 2002). En prepupa este estadio dura un promedio de dos días. Para pupar, se entierran en el suelo, entre 3 y 5 cm de profundidad, donde forman una cámara pupal, en la cual permanecen por 10 a 15 días aproximadamente, para posteriormente emerger como adulto en forma de mariposa de tamaño medio, de coloración gris oscuro, su aparición es nocturna y son fácilmente atraídas por las luces, (Coto Alfaro, 1998; Estrada, 2002).El ciclo completo dura aproxima-damente entre 35 y 40 días (1995; Mur-úa et al., 2003; Murúa & Virla, 2004).
¿Cuáles son las plantas hospederas preferentes del insecto en Améri-ca?
Se han identificado 186 plantas hospede-ras en S. frugiperda repartidas en 46 familias, las tres principales son la Poace-ae en un 35.5%, la Fabaceae en un 11.3 %, la Solanaceae y Asteraceae con un 4.3 %. La región más afectada fue Norteamé-rica con un 64%, y los principales culti-vos afectados en la región norte son: el maíz, sorgo, maní, caña de azúcar y arroz, en la región sur maíz, sorgo, arroz, poroto, algodón, alfalfa, tomate y papa. Y se considera que ciertas plantas como las pasturas y las gramíneas son malezas que representan un medio apro-piado para el desarrollo de poblaciones. (Betancourt y Scatoni, 1996).
El efecto del alimento va repercutir de manera trascendente en la eficacia bio-lógica del individuo dando como resulta-do consecuencias ecológicas y evolutivas, por lo que el rango de hospederos, es decir el conjunto de plantas que van a ser utilizadas por el insecto para su alimenta-ción son uno de los aspectos a considerar para el control de esta plaga.
La calidad de la planta puede afectar de manera positiva o negativa el desempeño del insecto, pues si la planta hospedera es pobre en nu-trientes el insecto va reabsorber los huevos para permitir la supervivencia (Murúa and Virla., 2004 ), la planta hospedera va jugar un papel impor-tante en la preferencia que presente el insecto por ella, pero no solo la planta si no las condiciones o la presencia de otros patógenos que invadan a dicho hospedero como las observaciones que se hicieron en larvas de tercer estadio que presenta-ban en su alimentación preferencia por las hojas de las plantas de ca-cahuate infectadas por moho blanco (S. rolfsii) las cuales tenían una supervivencia signifi-cativamente más alta, con pupas más pesados en un menor tiempo de pupación que los que se alimen-tan de plantas sanas (Cardoza y cols., 2002).
¿La planta huésped puede contribuir a la generación de biotipos en S. frugiperda?
Debido a que los lepidópteros son un orden de insectos que se ha caracterizado por presentar una amplia emisión adaptativa (Prowell 1998). Su cualidad polifagica ha resultado de interés en dife-rentes estudios ya que esto ha sido considerado como una alternativa que puede favorecer la coevo-lución entre los insectos y sus plantas hospederas permitiendo así una clasificación de los insectos dentro de diferentes categorías biológicas tales como “biotipos”, “razas hospederas” y finalmente, “especies”.
Un biotipo se basa en las siguientes características: a) poblaciones que presentan polimorfismos en pocos genes neutrales con poca evidencia de asociación con una planta hospedera, b) razas hospederas que en simpatría se diferenciaron genéticamente, pero que presentan poca evidencia de hibridación o flujo genético, c) verdaderas razas hospederas con diferenciación genética comprobada y con niveles significativos de hibridación, d) especies hermanas con diferenciaciones genéticas marcadas que mues-tran bajas tazas de hibridación o cuya hibridación no ocurre. (Dres y Mallet 2002)
Mientras que una raza es considerada y se diferencian como: a) poblaciones con marcada asociación a plantas hospederas, b) poblaciones que muestran fidelidad a su hospedero, c) poblaciones que coexis-ten en simpatría, por lo menos en parte de su rango de distribución, d) poblaciones que se diferencian genéticamente en más de un locus, e) muestran asociación a hospederos dentro de un amplio rango de distribución en el tiempo y el espacio, f) que muestran una correlación entre la preferencia hacia el hospedero y apareamiento asociativo y g) que muestran algún grado de hibridación o presentan flujo genético entre ellos (Dres y Mallet 2002).
En base a las características antes mencionadas S. frugiperda podría ser considerada como una especie, evolucionada de dos poblaciones que mostraron asociación a plantas hospederas como el maíz y el arroz, según (Nagoshi et al., 2007a, b, Nagoshi y Meagher 2003a, b, 2004, Pashley 1986, Prowell 1998).
Muestreos sistemáticos en diferentes zonas donde están en el mismo momento más de dos cultivos , se analizó su fluctuación poblacional durante varios años del insecto y se observó que mostraba preferencia por maíz, sorgo gramíneo, alfalfa y malezas a compara-ción de caña de azúcar y soya (Murúa et al., 2009). Las asociaciones con plantas hospederas muy posible-mente resultaron de un proceso de evolución gradual y lento en el cual una población ancestral sufre una o varias mutaciones neutrales que le permiten divergir en dos subpoblaciones ya sea en simpatría o alopatría.
Otro factor diferencial en los biotipos encontrados de S. frugiperda es el “aislamiento reproductivo preci-gotico y postcigotico” (Dres y Mallet. 2002).
El aislamiento precigotico se da por tres formas la primera de acuerdo a el temporal ya que el biotipo de maíz se aparea durante los primeros dos tercios de la noche mientras que el biotipo de arroz en el último tercio (Pashley et al. 1992), la segunda forma es su comportamiento donde rara vez se aparean hembras de maíz con los machos del biotipo de arroz, pero entre el mismo biotipo si se produce progenie (Pashley y Martin., 1987) y por último el aspecto ecológico de acuerdo a los dos biotipo de cada planta hospedera, por otra parte en relación con el aisla-miento postcigotico se demostró que existen barreras de aislamiento a nivel postcigotico entre los biotipos, esto debido a que las generaciones híbridas F1 y F2, entre estos biotipos, presentaron una reducción en el estado físico, fertilidad y viabilidad, comparado con sus líneas parentales de maíz y arroz la cual va ser parcial, esto debido a la forma en que se obtiene la progenie ya que en la cruza entre hembras del biotipo de maíz y hembras del biotipo de arroz van a presen-tar baja viabilidad en los híbridos de la F2, mientras que los individuos pertenecientes a la cruza reciproca va dar híbridos fértiles y viables ( Pashley y Martin., 1987, Nagoshi y Meagher., 2003, Velásquez-Vélez et al., 2011).
Un estudio realizado en México con el cruce de adultos entre poblaciones aisladas de cultivos de maíz, se determinaron el número de días a pupa, el peso de las mismas y su sobrevivencia. También se evaluó la compatibilidad reproductiva de los adultos y la susceptibilidad a controles con insecticidas quími-cos y Bacillus thuringiensis (Bt) donde utilizaron una cepa formada de poblaciones de Yucatán, Nuevo León y Aguascalientes localizadas en la Costa del Golfo de México contra una segunda forma-da en Colima y Sinaloa, localizadas en la Costa del Océano Pacífico, los cuales no produjeron progenie, por lo tanto se pudo concluir que el aislamiento geográfico juega un importante papel en el proceso de aisla-miento reproductivo del insecto, ya que el cruce entre poblaciones aisladas de distintos cultivos ha causado variación entre la proge-nie, los resultados sugieren que existen 2 cepas o biotipos entre las poblaciones de gusano cogollero del maíz (López-Edwards et al., 1999).
La especificidad planta-huésped refleja la adaptación nutricional, en el que las larvas en cepas de maíz y arroz muestran un ritmo más lento en el aumento de peso, más tiem-po de desarrollo, menor peso de las pupas, y la reducción de la supervivencia que cuando se crían en pasto bermuda, también reportaron reducciones en el peso de las larvas y pupas, pero no observaron diferen-cias en el tiempo de desarrollo o la supervivencia (Pashley 1988b; Pashley et al 1995; Veenstra et al., 1995, Whitford et al., 1988).
Un caso más de estudio que reforzó lo anterior es la evaluación de resistencia a insecticidas y la endotoxina Cry1AC en el que los biotipos han demostrado que su comportamiento difiere, en condiciones de laboratorio las larvas del biotipo del maíz han mostrado tener una mayor tolerancia a componentes de insecticidas como el carbaril, diazinon, cipermetrinas, metil paration y me-tiomil, además hacia cultivos de algodón transgénico con la endotoxina Cry1Ac de Bacillus thuringensis (Adamczyk et al., 1997), otro estudio muestra el comportamiento de resistencia de ambos biotipos a insecticidas en el que los dos difieren en su tolerancia hacia los insecticidas no sólo entre ellos sino con poblaciones venezolanas de S. frugiperda en maíz. Ríos Diez., en 2011, demostró que la LC50 de lambdacialotrina en el biotipo de arroz es de 31.16 ppm, SE = 3.13 e IC 95% entre 25.43-37.94, mientras que la LC50 de lambdacialotrina encontrada para el biotipo de maíz es de 45.01 ppm, SE = 7.16 e IC 95% entre 33.1-62.97 por lo tanto, el biotipo de maíz fue el más tolerante a este componente de insecticida comparado con el de arroz.
Estos eran los conocimientos previos pero no eran suficientes ya que la presencia de sus biotipos así deno-minados, no se podían distinguir entre unos y otros debido a que los biotipos eran casi idénticos morfológi-camente por lo que se dieron a la tarea de la implemen-tación de herramientas moleculares y bioquímicas para su identificación (Pashley, 1986) implementado el uso de aloenzimas para genotipificar las poblaciones de este insecto que mostraban una diferencia en su compor-tamiento alimenticio y fisiología hacia maíz y arroz en condiciones de laboratorio.
Estas poblaciones mostraron diferenciación genética también en un tipo de aloenzimas exhibiendo polimorfis-mos genéticos a nivel de 5 de estas aloenzimas, las cuales coinciden con cada biotipo de S. frugiperda de acuerdo a la planta hospedera de la que fueron colectadas, las aloenzimas B, C y D formaron parte exclusiva del bioti-po de maíz y las aloenzimas E y F fueron exclusivas del biotipo de arroz y los híbridos iban a presentar combina-ciones de estos en ambos biotipos (Pashley., 1986, Pashley et al., 2004, Prowell et al. 2004)
Estudios posteriores realizados en países como Estados Unidos, Jamaica, Guyana Francesa, Co-lombia e islas del Caribe por (Nagoshi y Meagher (2003 a, b, 2004, 2007 a, b, 2008), Prowell et al., 2004 y Vélez-Arango et al., 2008) demostraron que el rango de hospederos de estos biotipos es más amplio, ya que el biotipo maíz se encuentra en cultivos de maíz, secundariamente en algodón, y sorgo y el biotipo de arroz en arroz, pastos (Lobo, 2011), una vez que se realiza la identificación con aloenzimas, los estudios continuaron y surgieron otras técnicas moleculares como son los marcado-res este es el caso de una variación de la reacción en cadena de la polimerasa que es basada en la longitud de los fragmentos cuya técnica es PCR-RFLP (polimorfismos de longitud de los fragmentos de restricción) este se lleva a cabo a nivel del ADN mitocondrial con la enzima MspI que actúa en el gen de la citocromo oxidasa I (COI) produciendo así dos fragmentos digeridos de 497 pb y 72 pb en el biotipo maíz y ninguna diges-tión en el biotipo arroz (Levy et al. 2002; Meagher y Gallo-Meagher 2003).
Otra técnica molecular con marcadores es el uso de AFLP´s (polimorfismos de longitud de fragmentos amplificados) el cual consiste en combinar los métodos de PCR y análisis de fragmentos de res-tricción, y con el fin de detectar polimorfismos debidos a modificaciones en la secuencia de ADN , McMichael y Prowell 1999; Prowell et al. 2004 identificaron 19 bandas polimórficas en el biotipo arroz y 9 en el biotipo maíz, con una región en tándem del ADN nuclear denominada FR por las siglas en inglés y significan biotipo arroz que produ-ce amplificaciones de alto peso molecular (mayores a 500 pb) en dicho biotipo y de 0 a 3 bandas por debajo a las 500 pb en el biotipo maíz (Lu et al. 1994; Nagoshi y Meagher 2003 a, 2004; Machado et al. 2008).
La importancia de la caracterización de biotipos se ha presentado en estudios realizados en Estados Unidos, donde biotipos de S. frugiperda resultaron ser genéticamente distintos pero morfológicamente idénticos por lo que fueron reconocidas como dos posibles especies o razas hospederas en maíz y arroz (Dres and Mallet. 2002), demostraron que el rango de hospederos de estos biotipos es más amplio, ya que el biotipo maíz se encuentra en cultivos de maíz, secundariamente en algodón, y sorgo mien-tras que el biotipo arroz en arroz, pastos (Pashley 1986; Pashley 1998, Nagoshi y Meagher 2003, Nagoshi y Meagher 2004, Pashley et al. 2004) (Nagoshi y Meagher. 2004), (Pashley. 1986), (Nagoshi y Meagher., 2007).
Los estudios han sido evaluados en el fenotipo y el comportamiento del insecto y gracias a las herra-mientas moleculares los estudios aún persisten pues falta mucho por estudiar sobre esta plaga ya que de identificarse y determinar la presencia de estos biotipos será de gran ayuda para la implementación de nuevas estrategias de control de la plaga.

Divulgadores. Liz Ramiro + Departamento de Actuaría, Física y Matemáticas, Escuela de Ciencias, Universidad de las Américas Puebla.
Divulgadores. Francisco Alejandro Paredes Sánchez + Centro De Biotecnología Genómica, Instituto Politécnico Nacional.
Divulgadores. Alfredo De La Barrera González + ; Diego Alejandro Garnica Arriaga + ; Pedro Guevara Lopez + Escuela Superior De Ingeniería Mecánica Y Eléctrica ( Culhuacán ) - IPN, México.
Divulgadores. Elsa Verónica Herrera Mayorga + Centro De Biotecnología Genómica, Instituto Politécnico Nacional, Reynosa, Tamaulipas, México.
Divulgadores. Isela Madai Alba Moreno Tiss: + Centro de Biotecnología Genómica, Instituto Politécnico Nacional Reynosa, Tamaulipas, México.; .
Divulgadores. Julio Cesar Morales Hernández + ; Jorge Téllez López + Centro Universitario De La Costa, Universidad De Guadalajara, Puerto Vallarta, Jal.; Fátima Maciel Carrillo González + ; Víctor Manuel Cornejo López + ; Luis Manuel Farfan Molina + Cicese. Centro De Investigación Científica Y Estudios Superiores De Enseanda, Unidad De Meteorología, Cedela Paz, B.c.s..
Divulgadores. Francisco Angulo + .
Editorial. Redacción + 3ra Consejería.- Divulgación, Publicaciones y Medios.
Educadores. Cirilo Orozco Moret + Universidad De Carabobo. Unidad De Investigación En Educación Matemática Uiemat; Jesús Parra Arroyo + Universidad De Carabobo. Unidad De Investigación En Educación Matemática Uiemat.
Tecnólogos. Luis De Jesús Beltrán Sosa + ; Pedro Guevara López + Escuela Superior De Ingeniería Mecánica Y Eléctrica (culhuacán) - Ipn, México.
Tecnólogos. Jesús Audelo González + ; Pedro Guevara López + ; Gustavo Delgado Reyes + Escuela Superior De Ingeniería Mecánica Y Eléctrica (culhuacan) - Ipn, México.